seryum nadir toprak elementlerinin büyük ailesinde tartışmasız 'büyük kardeş'tir. Öncelikle, kabuktaki nadir toprak elementlerinin toplam bolluğu 238ppm'dir ve seryum 68ppm'de olup, toplam nadir toprak kompozisyonunun %28'ini oluşturur ve ilk sırada yer alır; İkincisi, seryum, itriyumun (1794) keşfinden dokuz yıl sonra keşfedilen ikinci nadir toprak elementidir. Uygulaması çok kapsamlıdır ve "seryum" durdurulamaz
Seryum Elementinin Keşfi

Carl Auer von Welsbach
Cerium, 1803 yılında Alman Kloppers, İsveçli kimyager J ö ns Jakob Berzelius ve İsveçli mineralog Wilhelm Hisinger tarafından keşfedildi ve isimlendirildi. Cerium olarak adlandırılır ve cevheri, 1801 yılında keşfedilen bir asteroit olan Ceres'in anısına cerit olarak adlandırılır. Aslında, bu tür seryum silikat, %66 ila %70 seryum içeren hidratlı bir tuzdur, geri kalanı ise kalsiyum, demir veitriyum.
Seryumun ilk kullanımı Avusturyalı kimyager Carl Auer von Welsbach tarafından icat edilen bir gaz şöminesiydi. 1885'te magnezyum, lantan ve itriyum oksit karışımını denedi, ancak bu karışımlar yeşil ışık yaydı ve başarılı olamadı.
1891'de, saf toryum oksidin mavi olmasına rağmen daha iyi bir ışık ürettiğini ve parlak beyaz ışık üretmek için Cerium(IV) oksitle karıştırıldığını buldu. Ek olarak, Cerium(IV) oksit toryum oksit yanması için bir katalizör olarak da kullanılabilir
seryum metali

★ Seryum, aktif özelliklere sahip sünek ve yumuşak gümüş beyazı bir metaldir. Havaya maruz kaldığında oksitlenir ve pas benzeri bir oksit tabakası oluşturur. Isıtıldığında yanar ve suyla hızla reaksiyona girer. Bir santimetre büyüklüğündeki seryum metal örneği yaklaşık bir yıl içinde tamamen aşınır. Hava, güçlü oksidanlar, güçlü asitler ve halojenlerle temasından kaçının.
★ Seryum esas olarak monazit ve bastnazitte, ayrıca uranyum, toryum ve plütonyumun fisyon ürünlerinde bulunur. Çevreye zararlıdır, su kütlelerinin kirlenmesine özel dikkat gösterilmelidir.
★ Seryum, Dünya kabuğunun 68ppm'sini oluşturan 26. en bol bulunan elementtir ve bakırdan (68ppm) sonra ikinci sıradadır. Seryum, kurşun (13pm) ve kalay (2,1ppm) gibi sıradan metallerden daha bol bulunur.
Seryum Elektron konfigürasyonu
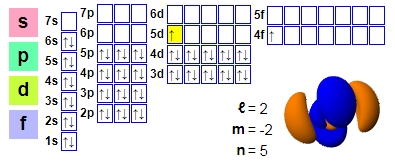
Elektronik düzenlemeler:
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p66s2 4f1 5d1
★ Seryum lantandan sonra yer alır ve seryumdan başlayarak 4f elektronuna sahiptir, bu da kimyasal reaksiyonlara katılmasını kolaylaştırır. Ancak seryumun 5d orbitali işgal edilmiştir ve bu etki seryumda yeterince güçlü değildir.
★ Çoğu Lantanit, değişken elektronik yapıya sahip seryum hariç, Valans elektronu olarak yalnızca üç elektron kullanabilir. 4f elektronlarının enerjisi, metal halinde delokalize edilmiş dış 5d ve 6s elektronlarının enerjisiyle hemen hemen aynıdır ve bu elektronik enerji seviyelerinin göreceli işgalini değiştirmek için yalnızca küçük bir enerji miktarı gerekir ve bunun sonucunda +3 ve +4'ün çift valansı elde edilir. Normal durum +3 valansıdır ve anaerobik suda +4 valansı gösterir.
Seryumun Uygulaması

★ Alaşım katkısı olarak ve seryum tuzları vb. üretiminde kullanılabilir.
★ Ultraviyole ve kızılötesi ışınları emen cam katkı maddesi olarak kullanılabilir ve Otomobil camlarında yaygın olarak kullanılır.
★ Mükemmel bir çevre koruma malzemesi olarak kullanılabilir ve şu anda en temsili olanı, büyük miktarda otomotiv egzoz gazının havaya atılmasını etkili bir şekilde önleyen otomotiv egzoz arıtma katalizörüdür.
★ Hafifnadir toprak elementleriBitki büyüme düzenleyicileri olarak esas olarak seryumdan oluşan bu ürünler, ürün kalitesini iyileştirebilir, verimi artırabilir ve ürün stres direncini artırabilir.
★ Seryum sülfür, pigmentlerde çevreye ve insana zararlı kurşun ve kadmiyum gibi metallerin yerini alabilir, plastikleri renklendirebilir, ayrıca kaplama ve mürekkep sanayinde kullanılabilir.
★Seryum(IV) oksitÖrneğin Kimyasal-mekanik parlatmada (CMP) parlatma bileşiği olarak kullanılabilir.
★ Seryum ayrıca hidrojen depolama malzemeleri, termoelektrik malzemeler, seryum tungsten elektrotlar, seramik kapasitörler, piezoelektrik seramikler, seryum silisyum karbür aşındırıcılar, yakıt hücresi hammaddeleri, benzin katalizörleri, kalıcı manyetik malzemeler, tıbbi malzemeler, çeşitli alaşımlı çelikler ve demir dışı metaller olarak da kullanılabilir.
Gönderi zamanı: Tem-03-2023